Une équipe de recherche de l’Institut de cardiologie de l’Université d’Ottawa (ICUO) dirigée par Yves Marcel , Ph. D., directeur du Laboratoire de biologie des HDL à l’ICUO, a découvert une nouvelle fonction à une voie cellulaire connue : la mobilisation et l’exportation du cholestérol des cellules. Cette fonction nouvellement découverte fait partie d’une ancienne voie, appelée « autophagie », qui est apparue chez les premiers organismes unicellulaires au cours de l’évolution.
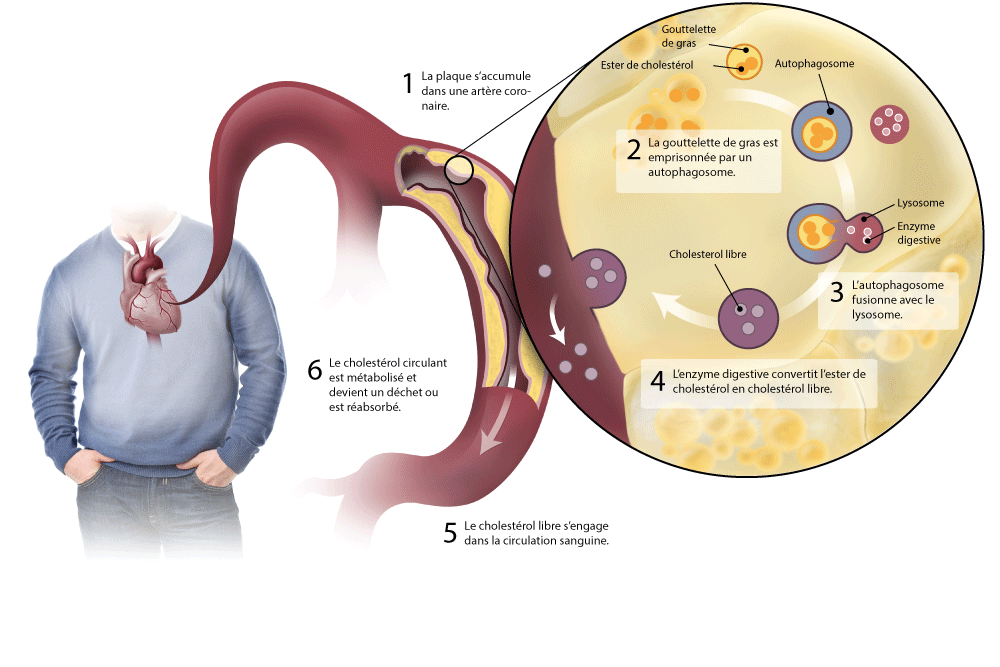
Des dépôts de gras provenant des surplus de cholestérol se forment le long des parois artérielles, causant des blocages et réduisant l’apport sanguin au cœur pour donner lieu à une maladie que l’on appelle « athérosclérose ». « Il est urgent de comprendre comment l’accumulation de cholestérol sur les artères peut être mise en échec », explique la chercheuse Mireille Ouimet, étudiante de cycle supérieur au laboratoire de M. Marcel et importante collaboratrice de l’étude.
La recherche de l’Institut de cardiologie a montré que l’autophagie pouvait isoler et digérer le cholestérol accumulé sur les parois des artères. « Ce processus facilite l’élimination du cholestérol et offre une cible entièrement nouvelle pour contrer l’athérosclérose, principale cause de crises cardiaques et d’accidents vasculaires cérébraux », précise M. Marcel.
Les détails de la recherche ont été publiés en ligne plus tôt cet été dans la revue scientifique Cell Metabolism (vol. 13, no 6, 2011, p. 655-667). L’étude montre comment l’accumulation de cholestérol elle-même déclenche l’autophagie, qui aide au fractionnement des gouttelettes de gras et au transport du cholestérol digéré vers le foie pour l’éliminer de l’organisme.
« Étant donné que cette voie favorise l’élimination du cholestérol de l’organisme et, par conséquent, réduit le risque de maladie du cœur, nos découvertes ouvrent de nouvelles perspectives pour éventuellement mettre l’athérosclérose en échec », explique M. Marcel. Il ajoute qu’il est possible que chez certains patients atteints de coro-naropathie, le mécanisme d’élimination du cholestérol artériel par la voie de l’autophagie soit altéré.
On savait déjà que l’autophagie jouait un rôle en récupérant des éléments toxiques des cellules et en favorisant la survie des cellules en cas de privation. Le terme « autophagie » est dérivé du grec ancien et signifie « se manger soi-même ». Au cours du processus d’autophagie, une membrane se forme autour des molécules dans la cellule ciblée pour les dégrader, puis les molécules nouvellement isolées sont livrées aux lysosomes des cellules, les structures qui digèrent les molécules en leurs éléments de base.
« C’est une voie qui est connue depuis longtemps, une voie qui est essentielle à la vie des cellules en général. Ici, nous avons trouvé une nouvelle application à cette voie, une application méconnue à ce jour », poursuit M. Marcel.
Il est intéressant de noter que si, dans le cadre de l’étude, une légère accumulation de cholestérol a déclenché le processus d’autophagie, une exposition chronique à un excès de lipides peut surcharger le processus. Pour l’avenir, il sera important de découvrir si cela se produit dans l’organisme humain quand l’athérosclérose se développe, et si l’accumulation à long terme du cholestérol peut surcharger ce système de décomposition naturelle. M. Marcel explique que si c’est le cas, le ciblage de cette voie pourrait s’avérer plus utile en médecine préventive que lorsque la maladie est bien installée.
On pourrait aussi découvrir des médicaments capables d’annuler l’inhibition de l’autophagie en présence de coronaropathie avancée, ajoute-t-il. Certains médicaments qui font déjà l’objet de tests pour traiter la maladie du cœur pourraient aider à activer l’autophagie en repoussant une protéine identifiée dans l’étude de M. Marcel.
M. Marcel poursuit en disant que l’activation contrôlée de l’autophagie peut être une nouvelle cible thérapeutique prometteuse pour la prévention et, éventuellement, le renversement de l’athérosclérose, mais il faut d’abord améliorer nos connaissances sur le fonctionnement du processus dans le corps humain au fil du temps.

Yves Marcel, Ph. D.
« Nos découvertes ouvrent de nouvelles perspectives pour éventuellement faire reculer l’athérosclérose. »
- Directeur, Programme d’athérosclérose, génétique et biologie cellulaire; directeur, Laboratoire de biologie des HDL, Institut de cardiologie de l’Université d’Ottawa
- Professeur, Département de pathologie et de médecine de laboratoire; professeur, Département de biochimie, de microbiologie et d’immunologie de l’Université d’Ottawa
- Recherche : HDL, structure de l’apolipoprotéine A-I et transport inverse du cholestérol; interaction de l’apolipoprotéine E (apoE) avec les éléments de la matrice extracellulaire hépatique; nature et rôle de l’apoE dans le métabolisme des lipoprotéines à la surface cellulaire.
L’étude en cours permet de mieux comprendre les complexités biochimiques sousjacentes impliquant le cholestérol. Ce dernier est important pour la structure cellulaire, mais les problèmes surviennent quand de trop grandes quantités de cholestérol se déposent à l’intérieur des parois des artères coronaires, l’origine de la maladie coronarienne.
La carrière de chercheur de M. Marcel a porté principalement sur les lipoprotéines, mécanisme biochimique qui transporte le cholestérol et les matières grasses dans l’organisme. En 1997, il a reçu la plus importante médaille d’honneur de la Société royale du Canada pour sa contribution aux sciences médicales, incluant la recherche liée aux voies des acides gras polyinsaturés. Il s’agissait de la Médaille McLaughlin, considérée comme l’un des honneurs les plus prestigieux au pays soulignant l’excellence en recherche.

